Реакције једињења живе
Метална жива и њена једињења су веома токсични за живе организме. Ово посебно важи за једињења која су веома растворљива у води. Мора се обратити велика пажња када се експериментише са комбинацијама овог јединственог елемента (жива је једини метал који је течан на собној температури). Усклађеност са основним прописима хемичара? омогућиће вам безбедно спровођење неколико експеримената са једињењима живе.
У првом експерименту добијамо алуминијумски амалгам (раствор овог метала у течној живи). Жива (ИИ) раствор Хг нитрат (В) Хг (НО3)2 и комад алуминијумске жице (слика 1). Алуминијумска шипка (пажљиво очишћена од наслага) ставља се у епрувету са раствором растворљиве соли живе (слика 2). После неког времена можемо посматрати ослобађање мехурића гаса са површине жице (фотографије 3 и 4). Након уклањања шипке из раствора, испоставља се да је глина прекривена пухастим премазом, а поред тога видимо и куглице металне живе (фотографије 5 и 6).
Хемија – искуство комбиновања живе
У нормалним условима, површина алуминијума је обложена слојем алуминијум-оксида који се чврсто уклапа.2O3ефикасно изолује метал од агресивних утицаја околине. Након чишћења и потапања штапа у раствор живине соли, Хг јони се истискују2+ активнији алуминијум
Жива таложена на површини штапа формира амалгам са алуминијумом, што отежава пријањање оксида на њега. Алуминијум је веома активан метал (реагује са водом и ослобађа водоник – примећују се мехурићи гаса), а његова употреба као конструктивног материјала је могућа због густог оксидног премаза.
У другом експерименту ћемо детектовати амонијум НХ јоне.4+ користећи Неслеров реагенс (немачки хемичар Јулијус Неслер га је први употребио у анализи 1856).
Експериментисати са реакцијом хмеља и једињења живе
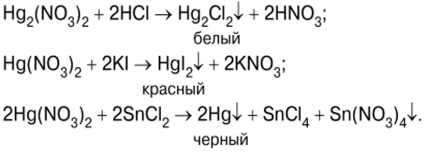
Тест почиње преципитацијом живиног(ИИ) јодида ХгИ.2, након мешања раствора калијум јодида КИ и живиног (ИИ) нитрата (В) Хг (НО3)2 (слика 7):
Наранџасто-црвени преципитат ХгИ2 (слика 8) затим третиран вишком раствора калијум јодида да би се добило растворљиво комплексно једињење формуле К2ХгИ4 ? Калијум тетраиодеркурат (ИИ) (слика 9), који је Несслеров реагенс:
Са добијеним једињењем можемо детектовати амонијум јоне. И даље ће бити потребни раствори натријум хидроксида НаОХ и амонијум хлорида НХ.4Цл (слика 10). Након додавања мале количине раствора амонијумове соли у Неслеров реагенс и алкализације медијума са јаком базом, посматрамо формирање жуто-наранџасте боје садржаја епрувете. Тренутна реакција се може написати као:
Добијено једињење живе има сложену структуру:
Високо осетљиви Несслеров тест се користи за откривање чак и трагова амонијумових соли или амонијака у води (нпр. вода из чесме).

